1. Introduction
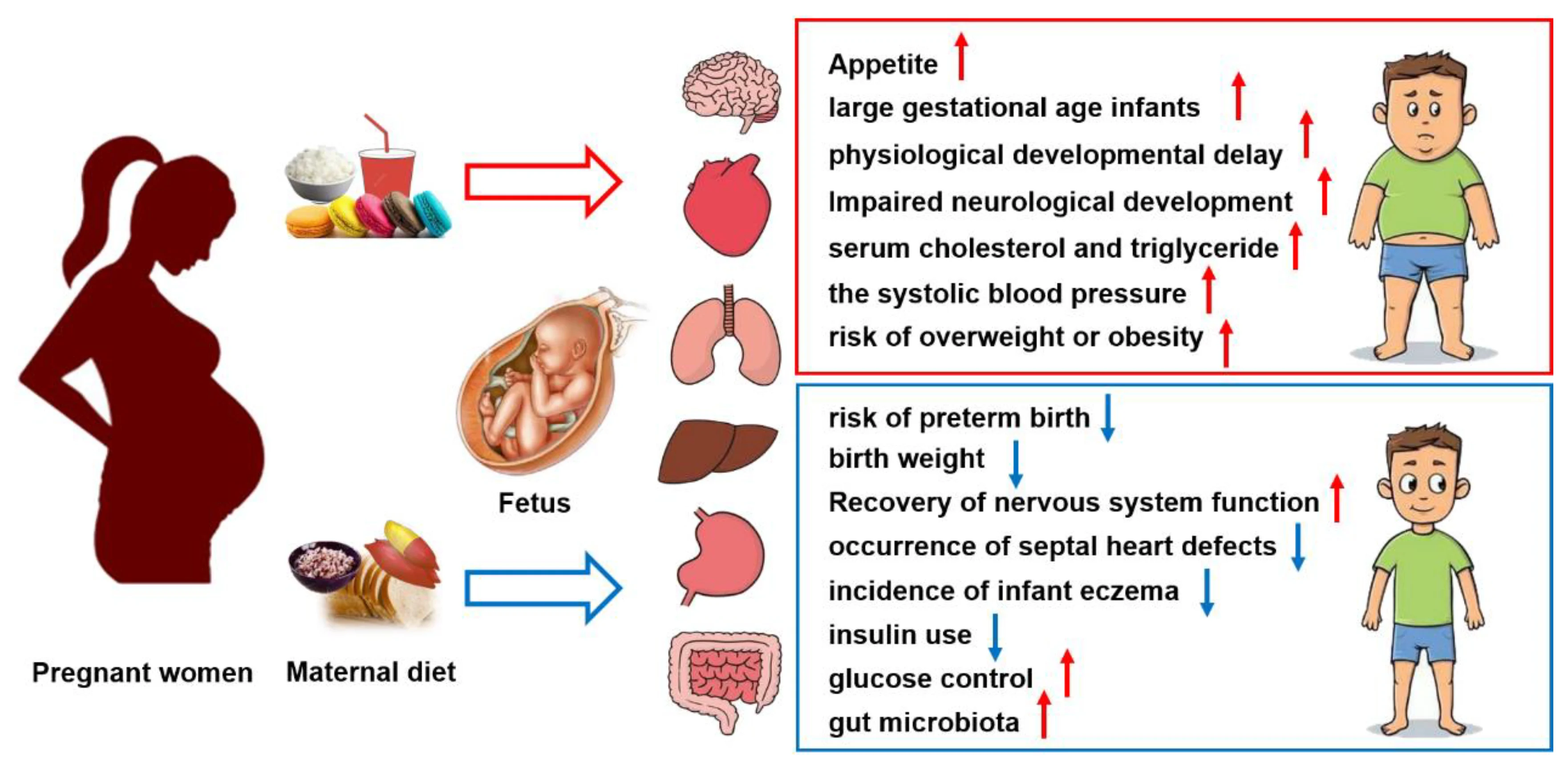
Les maladies chroniques représentent l’une des principales causes de mortalité dans le monde. Il a été suggéré que des pathologies liées à la grossesse telles que le diabète gestationnel (DG), l’obésité maternelle (OM) et le retard de croissance intra-utérin (RCIU) induisent un environnement intra-utérin défavorable, augmentant ainsi la prédisposition de l’enfant à développer des maladies chroniques plus tard dans sa vie.
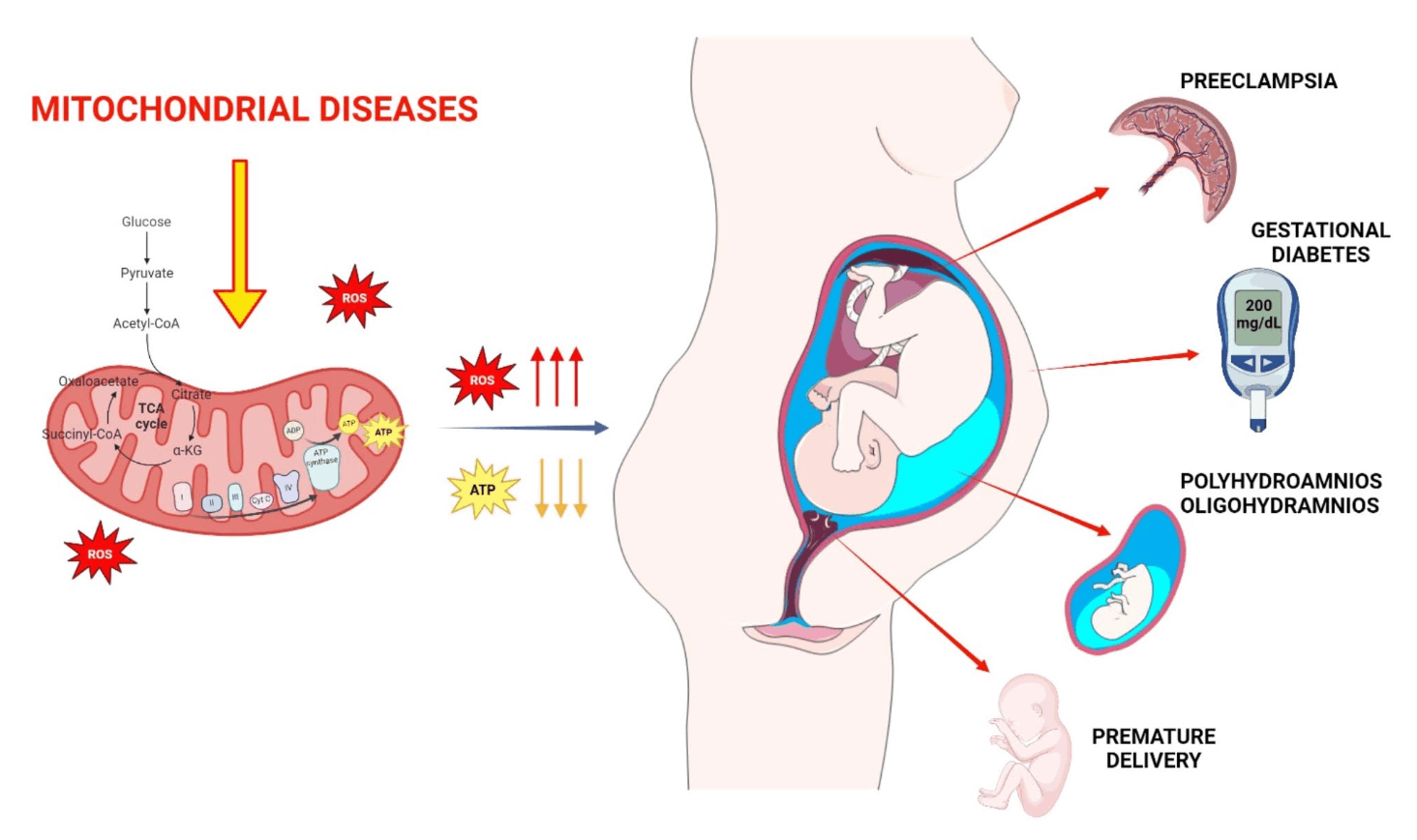
Des recherches ont suggéré que la fonction mitochondriale et le stress oxydatif pourraient jouer un rôle dans la programmation des maladies chroniques. Cette approche pourrait atténuer les risques de maladies chroniques liés au développement foetal et constituer une intervention probable en matière de prévention des maladies.
Le diabète gestationnel (DG) se définit par un état d’hyperglycémie et d’intolérance au glucose détecté pour la première fois au cours du deuxième ou du troisième trimestre de la grossesse.
Il est bien établi que le DG est la complication de grossesse la plus fréquente.
Parmi les facteurs de risque identifiés pour le développement du DG figurent
- l’âge maternel et l’obésité, les femmes enceintes obèses présentant un risque 2,4 fois plus élevé de développer un DG.
- L’obésité maternelle (OM) représente elle-même une complication de grossesse très fréquente. On estime qu’environ 50 % des grossesses surviennent chez des femmes en surpoids ou obèses.
- Le DG et l’OM contribuent tous deux à un risque accru d’induire un environnement fœto-placentaire semblable à une hypoxie prolongée de même que d’autres facteurs tels que le tabagisme maternel, un dysfonctionnement vasculaire et une carence en nutriments chez la mère.
Ces conditions peuvent aggraver un développement et une croissance fœtale insuffisants, une affection appelée retard de croissance intra-utérin (RCIU).
Ces troubles liés à la grossesse induisent des adaptations structurelles, fonctionnelles et métaboliques dans plusieurs organes dès le stade fœtal. Dans ce contexte, il a été suggéré que le stress oxydatif et le dysfonctionnement mitochondrial pourraient constituer des mécanismes clés de la programmation développementale dans les troubles liés à la grossesse. Par conséquent, ces mécanismes pourraient représenter des cibles stratégiques pour moduler la programmation des maladies chroniques non transmissibles chez l’enfant pendant la grossesse.
2. Programmation développementale des maladies chroniques par les troubles associés à la grossesse
2.1. Rôle (patho)physiologique des espèces réactives de l’oxygène dans le développement fœtal
2.2. Impact des troubles associés à la grossesse sur le stress oxydatif et la fonction mitochondriale des organes foetaux
La grossesse est un état de forte demande énergétique principalement assurée par l’activité métabolique fœto-placentaire. Les mitochondries sont des acteurs clés du métabolisme et l’une des principales sources d’énergie cellulaire. Ce sont des organites très sensibles aux besoins énergétiques. Par conséquent, la fonction mitochondriale placentaire peut être modulée en réponse à un environnement intra-utérin défavorable. Dans les troubles liés à la grossesse, les dysfonctionnements métaboliques placentaires sont largement documentés et peuvent avoir des conséquences durables pour l’enfant tant pendant la période prénatale que postnatale.
L’état d’hyperglycémie caractéristique du diabète gestationnel (DG) peut altérer la structure et la fonction mitochondriales placentaires. En effet, les placentas de femmes présentant un DG montraient des mitochondries gonflées et altérées, certaines étant complètement détruites.
Les mitochondries étant des organites très dynamiques, dont le nombre, la morphologie, le réseau et la taille varient en fonction des besoins énergétiques cellulaires, leur forme et leur fonction sont étroitement liées.
Les cytotrophoblastes humains issus de grossesses avec DG présentent une diminution de la capacité respiratoire mitochondriale maximale et une baisse du taux de production d’ATP, ce qui souligne le dysfonctionnement bioénergétique mitochondrial induit par le DG.
Le diabète maternel, qu’il s’agisse d’un diabète de type 2 prégestationnel ou d’un diabète gestationnel (DG) altère la biogenèse mitochondriale placentaire (formation de nouvelles mitochondries) avec une diminution des niveaux d’expression du facteur de transcription mitochondrial A (TFAM).
Outre cette altération de la biogenèse mitochondriale placentaire le DG induit une modification de la dynamique mitochondriale. Des études chez l’humain rapportent soit une augmentation, soit une diminution des événements de fusion mitochondriale placentaire. Ces événements de fusion sont considérés comme essentiels au maintien du nombre de copies d’ADN mitochondrial (ADNmt).
Par ailleurs, un stress oxydatif placentaire a été fréquemment rapporté dans les placentas de femmes atteintes de diabète gestationnel. Bien que les espèces réactives de l’oxygène (ROS) soient produites par plusieurs sources, les mitochondries sont considérées comme l’une des principales.
Les grossesses humaines atteintes de diabète gestationnel présentent une augmentation des biomarqueurs placentaires du stress oxydatif, tels que le malondialdéhyde (MDA) une réduction des défenses antioxydantes (diminution de l’activité de la catalase (CAT) et de la glutathion peroxydase (GPx).
Outre le placenta, les cellules souches mésenchymateuses du cordon ombilical humain (hUC-MSC) de femmes atteintes de diabète gestationnel présentent une production accrue d’espèces réactives de l’oxygène (ROS).
Étant donné que les cellules souches mésenchymateuses (MSC) sont multipotentes, elles peuvent se différencier en une grande variété de types cellulaires au cours du développement fœtal, notamment en adipocytes, cardiomyocytes, myocytes et neurones. Un dysfonctionnement des MSC peut induire des dysfonctionnements cellulaires et organiques chez la descendance, ce qui peut ultérieurement accroître le risque de maladie cœliaque.
Les atteintes des organes de la descendance liées au diabète gestationnel restent peu étudiées dans la littérature ce qui nécessite des études plus nombreuses et de plus grande envergure. Néanmoins, les données disponibles, tant chez l’humain que chez des modèles animaux murins, suggèrent que le diabète gestationnel peut induire des altérations mitochondriales dans les préadipocytes, le pancréas, le foie et le cœur du foetus.
Par ailleurs, des études chez le rongeur ont montré la présence d’un stress oxydatif dans les tissus de la progéniture de mères atteintes de diabète gestationnel, notamment dans le cortex cérébral, caractérisé par une augmentation des ROS, une peroxydation lipidique accrue et une diminution de l’activité de la CAT, comparativement au groupe témoin, chez les rats mâles et femelles adultes issus de mères traitées à la streptozotocine (utilisé dans les études animales afin d’induire un diabète expérimental.
Le milieu métabolique intra-utérin diffère entre le diabète gestationnel et l’obésité morbide. Néanmoins, malgré ces différences, le milieu intra-utérin de l’obésité morbide est également hyperglycémique et pro-oxydant. Semblables aux placentas humains atteints de diabète de grossesse, les placentas humains Mdes mères obèses présentent un dysfonctionnement mitochondrial, c’est-à-dire une biogenèse perturbée et une bioénergétique (diminution de l’activité du complexe I et diminution des niveaux d’ATP) entrainant une formation excessive de ROS et des dommages oxydatifs et des défenses antioxydantes plus faibles (diminution de l’activité de la SOD, diminution des niveaux d’expression de la GPx-4) soit dans le tissu placentaire humain entier ou dans les cytotrophoblastes.
Il a été suggéré que cet environnement métabolique modifié contribue au dysfonctionnement métabolique placentaire induit par l’obésité maternelle, soulignant l’impact potentiel du dysfonctionnement mitochondrial placentaire induit par cette situation sur la croissance fœtale.
L’exposition fœtale prolongée à l’hypoxie induite par le diabète gestationnel (DG) et l’obésité maternelle peut entraîner un retard de croissance intra-utérin (RCIU). Des études ont notamment mis en évidence des points communs entre le DG, l’obésité maternelle et le RCIU au niveau placentaire soulignant une altération de la fonction mitochondriale et augmentation du contenu placentaire en ATP et un stress oxydatif et augmentation de l’expression de la catalase possiblement comme mécanisme compensatoire contribuant au dysfonctionnement métabolique du placenta humain en cas de RCIU.
Chez les enfants nés de mères présentant un retard de croissance intra-utérin (RCIU), un dysfonctionnement mitochondrial est observé dans plusieurs organes, notamment le cœur et le foie et ce dysfonctionnement est rapporté de manière hétérogène selon l’âge fœtal ou néonatal. De plus, un stress oxydatif est également présent dans le cerveau et le cœur de ces enfants ainsi que dans le foie et ce à différents stades de la vie fœtale ou néonatale.
3. Antioxydants et activité mitochondriotrope des antioxydants naturels et synthétiques
L’obésité maternelle, le diabète gestationnel et le retard de croissance intra-utérin sont responsable d’une perturbation de la programmation du développement foetal impliquant une interaction complexe de mécanismes tissulaires spécifiques et généraux où les modifications épigénétiques, les altérations mitochondriales et le stress oxydatif jouent un rôle prépondérant.
De plus, les dysfonctionnements tissulaires et mitochondriaux, fréquemment consécutifs à une exacerbation du stress oxydatif associé à la grossesse, entraînent un dysfonctionnement métabolique maternel dans un cercle vicieux.
Ainsi, une supplémentation maternelle en antioxydants représente une approche prometteuse pour atténuer les effets de la programmation développementale chez la descendance exposée à des troubles liés à la grossesse, caractérisés par une production élevée d’espèces réactives de l’oxygène (ROS). L’administration d’antioxydants a été étudiée comme une stratégie possible, permettant aux antioxydants exogènes, d’origine alimentaire ou synthétique, d’agir en synergie avec les antioxydants endogènes pour rétablir l’homéostasie redox.
3.1. Antioxydants naturels
3.1.1. Antioxydants endogènes
Dans des conditions physiologiques, l’organisme humain produit naturellement des molécules antioxydantes pour éliminer l’excès d’espèces réactives de l’oxygène (ROS), prévenant ainsi le stress oxydatif et les lésions tissulaires qui en découlent.
Le système de défense antioxydant endogène comprend :
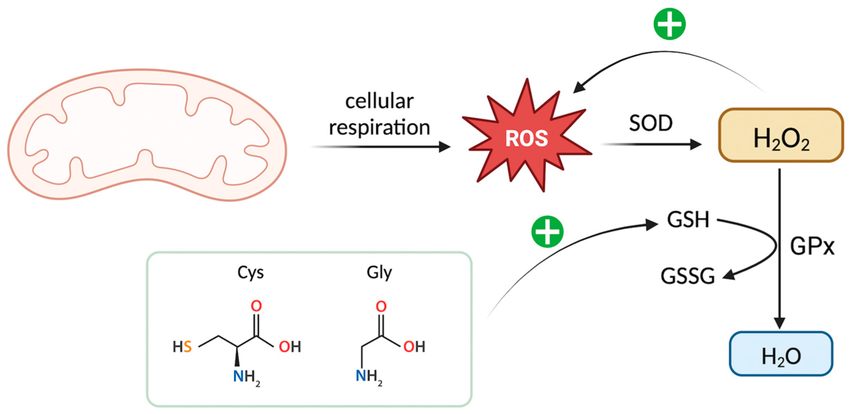
- des enzymes antioxydantes telles que la superoxyde dismutase (SOD), la catalase (CAT) et la glutathion peroxydase (GPx),
- le glutathion,
- des protéines comme la ferritine
- des piégeurs de radicaux libres de faible poids moléculaire comme la coenzyme Q10 (CoQ10), qui contribuent au maintien de l’homéostasie redox cellulaire.
La SOD constitue la première ligne de défense antioxydante en convertissant l’anion superoxyde en peroxyde d’hydrogène (H₂O₂ ). La CAT et la GPx , quant à elles, interviennent dans la réduction du H₂O₂ en eau et en oxygène moléculaire.
De fait, les antioxydants enzymatiques sont plus efficaces pour lutter contre le stress oxydatif grâce à leur capacité à éliminer les ROS, prévenant ainsi les dommages aux protéines, à l’ADN et aux lipides.
En revanche, les antioxydants non enzymatiques peuvent agir en :
- capturant les ions de métaux de transition, principalement responsables de la production d’espèces réactives de l’oxygène, ou en stockant les ions métalliques nécessaires à la synthèse d’enzymes contenant des ions métalliques (protéines liant les métaux, par exemple la ferritine et la transferrine).
- De plus, ils peuvent piéger les radicaux libres (par exemple le glutathion et l’acide urique) et interférer directement avec les étapes d’initiation et de propagation du processus de peroxydation, agissant ainsi comme inhibiteurs de la peroxydation lipidique et protégeant les cellules des dommages. Ils jouent un rôle important dans le métabolisme, comme c’est le cas de la coenzyme Q10, un antioxydant endogène liposoluble naturel situé dans la membrane mitochondriale interne.
3.1.2. Antioxydants alimentaires
3.2. Antioxydants synthétiques
Ces composés ont été développés pour pallier principalement les limitations pharmacologiques de certains antioxydants.
MitoTEMPO et MitoQ sont des exemples d’antioxydants mitochondriaux efficaces, concus pour cibler spécifiquement les mitochondries.
Antioxydants ciblant les mitochondries
4. Explorer le rôle de la supplémentation en antioxydants alimentaires pendant la grossesse dans la prévention des maladies non transmissibles chez la descendance
L’état nutritionnel maternel est primordial avant et après la conception ainsi que pendant toute la durée de l’allaitement pour un développement fœtal optimal. Il est démontré que des ajustements alimentaires chez la mère comme le maintien d’un apport équilibré en énergie et en protéines, peuvent être bénéfiques durant ces phases afin de réduire le risque de perte fœtale, de mortinatalité et de mortalité périnatale.
4.1. Vitamines
Le débat sur la supplémentation vitaminique pendant la grossesse est vaste.
Ainsi, l’innocuité et l’efficacité de la supplémentation en antioxydants doivent être soigneusement évaluées afin de déterminer les types, les dosages et le moment optimaux de cette supplémentation pour les différentes populations de femmes enceintes.
À la lumière de ces résultats et compte tenu du fait que les essais cliniques impliquant des femmes enceintes font toujours l’objet de controverses, il est de plus en plus nécessaire d’explorer des options de supplémentation nouvelles, sûres, efficaces et bénéfiques pendant la grossesse.
4.2. Resvératrol
Le resvératrol atténue les mécanismes de résistance à l’insuline, les processus inflammatoires et le stress oxydatif dans le foie maternel.
L’administration de resvératrol induit chez la progéniture de souris atteintes de diabète gestationnel une régulation négative de la voie de la gluconéogenèse.
4.3. Curcumine
L’administration de curcumine chez des souris gravides suivant un régime riche en graisses a démontré sa capacité à améliorer la sensibilité à l’insuline et à activer la thermogenèse dans le tissu adipeux brun (TAB) et le tissu adipeux blanc (TAB) chez leurs descendants mâles.
Ces résultats favorables contribuent probablement à l’amélioration de la fonction mitochondriale et de la dépense énergétique chez les descendants de mères suivant un régime riche en graisses, fonctions qui seraient altérées par la suralimentation.
La curcumine améliore également les symptômes du diabète gestationnel (DG) tels que l’hyperglycémie et l’insulinorésistance.
La curcumine a également des propriétés anti inflammatoire en inhibant le NFKB.
4.4. La N Acetyl Cystéine (NAC)
Dans un modèle murin d’obésité induite par un régime obésogène, une supplémentation orale maternelle en NAC a diminué le tissu adipeux blanc (WAT), la stéatose hépatique et l’inflammation tout en augmentant l’expression des gènes thermogéniques dans le tissu adipeux brun (BAT).
De plus, une augmentation de l’activité de la GPx a été observée, soulignant l’effet antioxydant potentiel d’une supplémentation maternelle en NAC sur la santé postnatale de la descendance.
L’administration orale de NAC par gavage semble diminuer le stress oxydatif maternel en stimulant les défenses antioxydantes hépatiques, notamment l’activité de la SOD (SuperOxydeDysmutase), de la GPx (Gluthationperoxydase) et de la CAT (Catalase), ainsi que les taux de GSH et en réduisant les taux de MDA (malondialdéhyde) dans un modèle murin de diabète gestationnel.
Conclusion
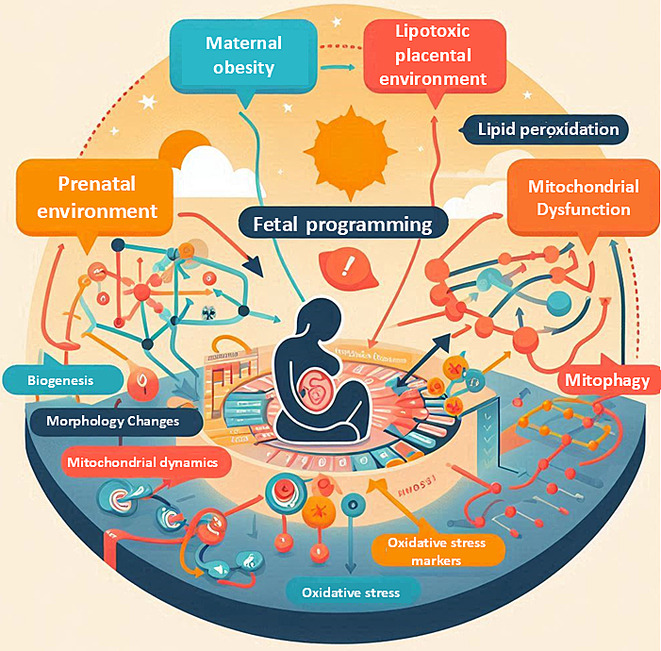
L’obésité maternelle perturbe profondément la fonction mitochondriale placentaire, comme en témoignent des modifications significatives de la teneur en ADN mitochondrial de l’expression des protéines liées à la dynamique et à la biogenèse mitochondriales à la mitophagie et au stress oxydatif.
Ces perturbations moléculaires peuvent créer un environnement intracellulaire lipotoxique, induisant un dysfonctionnement cellulaire au niveau du placenta et des modifications épigénétiques chez le fœtus. De telles altérations ont des conséquences importantes, pouvant se manifester par des maladies métaboliques, cardiovasculaires et dégénératives durant l’enfance et même à l’âge adulte.
Bibliographie
-
Nurturing through Nutrition: Exploring the Role of Antioxidants in Maternal Diet during Pregnancy to Mitigate Developmental Programming of Chronic Diseases. Mariana S. Diniz, Carina C. Magalhães, Carolina Tocantins, Luís F. Grilo, José Teixeira and Susana P. Pereira. Nutrients2023, 15(21), 4623;
-
Maternal Dietary Carbohydrate and Pregnancy Outcomes: Quality over Quantity. Lamei Xue, Xiaofang Chen, Juan Sun, Mingcong Fan, Haifeng Qian and Li Wang. Nutrients2024, 16(14), 2269;
-
Fetal and obstetrics manifestations of mitochondrial diseases. Alessia Adelizzi1, Anastasia Giri2, Alessia Di Donfrancesco, Simona Boito, Alessandro Prigione, Emanuela Bottani, Valentina Bollati, Valeria Tiranti, Nicola Persico and Dario Brunetti. Journal of Translational Medicine. (2024) 22:853
-
Role of Oxidative Stress in Tuberculosis Meningitis Infection in Diabetics. Inès Navasardyan, Stéphanie Yeganyan, Helena Nguyen. biomédicaments2023 , 11 (9), 2568;
-
Targeting Oxidative Stress with Polyphenols to Fight Liver Diseases. Ivo F. Machado, Raul G. Miranda, Daniel J. Dorta, Anabela P. Rolo and Carlos M. Palmeira. Antioxidants2023, 12(6), 1212;
-
Mitochondria-Targeted Antioxidants, an Innovative Class of Antioxidant Compounds for Neurodegenerative Diseases: Perspectives and Limitations. Matteo Fields, Annalisa Marcuzzi, Arianna Gonelli, Claudio Celeghini, Natalia Maximova and Erika Rimondi. Int. J. Mol. Sci.2023, 24(4), 3739;
-
Mitochondrial dynamics, biogenesis, mitophagy and oxidative stress in gestational obesity: A review. Karenth Milena Rodríguez-Córdoba, Sofia Agreda Soto, Jenniffer Alejandra Castellanos Garzón, Maria Carolina Pustovrh-Ramos. Endocrine and Metabolic ScienceVolume 17, March 2025, 100205